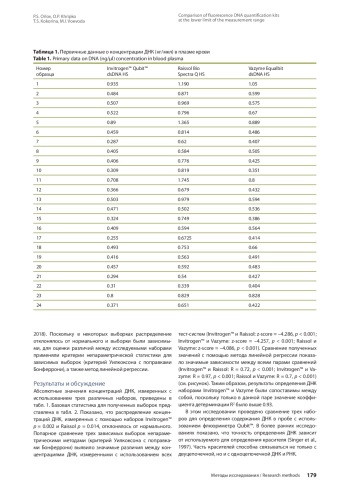
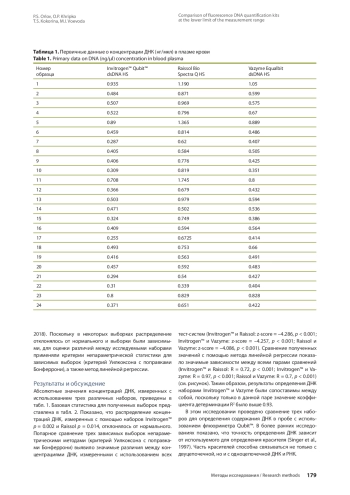
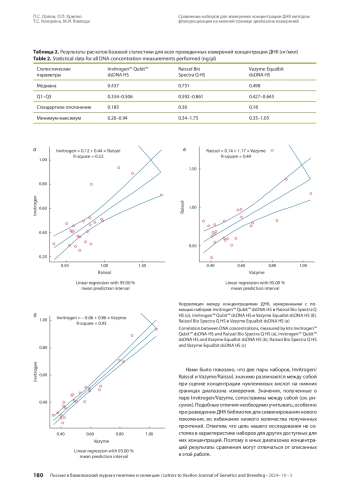
В настоящее время необходима замена расходных материалов и реагентов от производителей из США и Евросоюза. В этой работе проводится сравнение наборов для измерения концентрации ДНК методом флюоресценции от производителей из Российской Федерации (Raissol Bio Spectra Q HS) и КНР (Vazyme Equalbit dsDNA HS) с набором производства США (Invitrogen™ Qubit™ dsDNA HS). С использованием данных наборов измерена концентрация ДНК 24 образцов плазмы периферической крови человека. Установлено, что абсолютные значения концентраций ДНК, определенных с помощью трех наборов, имели статистически значимые различия при парных сравнениях. При этом наибольшее медианное значение концентрации ДНК было зафиксировано с применением набора Raissol Bio Spectra Q HS (0.751 нг/мкл) по сравнению с наборами Vazyme Equalbit dsDNA HS (0.498 нг/мкл) и Invitrogen™ Qubit™ dsDNA HS (0.437 нг/мкл). Регрессионный анализ выявил значимые зависимости между концентрациями ДНК, измеренными с помощью различных наборов. Наибольший коэффициент детерминации (R2 = 0.93) был определен при сравнении значений концентраций ДНК, измеренных с использованием наборов Invitrogen: Vazyme. Для оставшихся двух пар, Invitrogen: Raissol и Vazyme: Raissol, коэффициенты детерминации не превышали значения в 0.521. Таким образом, измеренные концентрации ДНК с применением указанных наборов оказались сопоставимы между собой и могут быть пересчитаны относительно друг друга с помощью уравнений регрессии.
Идентификаторы и классификаторы
В настоящее время секвенирование нового поколения широко вошло в повседневную клиническую практику для диагностики и определения тактики лечения. Качество выделенных нуклеиновых кислот в большой степени зависит от различных преаналитических процедур, включающих фиксацию и доставку в лабораторию, а также среды, в которую был забран материал. Поэтому точность количественного определения ДНК играет ключевую роль в успешном проведении тестов. Количество ДНК в растворе может быть измерено при помощи спектрофотометрии (Glasel, 1995; Huberman, 1995; Manchester, 1995), однако данный метод имеет ряд существенных недостатков. Во-первых, поглощение в ультрафиолетовом спектре не является избирательным в отношении ДНК, РНК или белка. во-вторых, поглощение находится в сильной зависимости от различных загрязнителей. В-третьих, точность измерения таким методом, как правило, недостаточна при низких концентрациях ДНК. В качестве альтернативного метода определения количества ДНК в растворе, не имеющего таких недостатков, широко используется метод количественного анализа на основе флюоресценции (Le Pecq, Paoletti, 1966; Kapuscinski, 1995; Singer et al., 1997; Jones et al., 1998).
Список литературы
1. Алгоритмы биологической статистики: учебн.-метод. пособие / сост. С.П. Кожевников. Ижевск: Изд. центр “Удмуртский университет”, 2018.
Algorithms of Biological Statistics: Educational Method: allowance / comp. S.P. Kozhevnikov. Izhevsk: Publ. House Center “Udmurt University”, 2018.
2. Телышева Е.Н. Свободно-циркулирующая ДНК плазмы крови. Возможности применения в онкологии. Вестник Российского научного центра рентгенорадиологии Минздрава России. 2017;17(2):2. EDN: ZGIDKR
Telysheva E.N. Free-circulating DNA of blood plasma. Possible applications in oncology. Vestnik Rossijskogo Nauchnogo Tsentra Rentgenoradiologii Minzdrava Rossii = Bulletin of the Russian Scientific Center of Radiology of the Ministry of Health of Russia. 2017;17(2):2. (in Russian).
3. Bonin S., Hlubek F., Benhattar J., Denkert C., Dietel M., Fernandez P.L., Höfler G., Kothmaier H., Kruslin B., Mazzanti C.M., Perren A., Popper H., Scarpa A., Soares P., Stanta G., Groenen P.J. Multicentre validation study of nucleic acids extraction from FFPE tissues. Virchows Arch. 2010;457(3):309-317. DOI: 10.1007/s00428-010-0917-5 EDN: NYZHMX
4. Glasel J.A. Validity of nucleic acid purities monitored by 260 nm/280 nm absorbance ratios. BioTechniques. 1995;18:62-63.
5. Hoeter K., Neuberger E., Fischer S., Herbst M., Juškevičiūtė E., Enders K., Rossmann H., Sprinzl M.F., Simon P., Bodenstein M., Schaefer M. Evidence for the utility of cfDNA plasma concentrations to predict disease severity in COVID-19: a retrospective pilot study. PeerJ. 2023;11:e16072. DOI: 10.7717/peerj.16072 EDN: OHIDDV
6. Huberman J.A. Importance of measuring nucleic acid absorbance at 240 nm as well as at 260 and 280 nm. Biotechniques. 1995;18:636.
7. Jones L.J., Yue S.T., Cheung C.Y., Singer V.L. RNA quantitation by fluorescence-based solution assay: RiboGreen reagent characterization. Anal. Biochem. 1998;265:368-374. DOI: 10.1006/abio.1998.2914
8. Kapuscinski J. DAPI: A DNA-specific fluorescent probe. Biotech. Histochem. 1995;70(5):220-233. DOI: 10.3109/10520299509108199
9. Le Pecq J.B., Paoletti C. A new fluorometric method for RNA and DNA determination. Anal. Biochem. 1966;17:100-107. DOI: 10.1016/0003-2697(66)90012-1
10. Manchester K.L. Value of A260/A280 ratios for measurement of purity of nucleic acids. Biotechniques. 1995;19:208-210.
11. Mishra S., Dubey D.B., Agarwal K., Dubey D.B., Verma S., Shabbir N., Kushwaha R., Reddy D.H., Singh U.S., Ali W. Circulating cell-free DNA level in prediction of COVID-19 severity and mortality: correlation of with haematology and serum biochemical parameters. Indian J. Clin. Biochem. 2023;38(2):172-181. DOI: 10.1007/s12291-022-01082-4 EDN: IEBOSF
12. Sah S., Chen L., Houghton J., Kemppainen J., Marko A.C., Zeigler R., Latham G.J. Functional DNA quantification guides accurate nextgeneration sequencing mutation detection in formalin-fixed, paraffin-embedded tumor biopsies. Genome Med. 2013;5:77. DOI: 10.1186/gm481 EDN: LUQYDJ
13. Singer V.L., Jones L.J., Yue S.T., Haugland R.P. Characterization of Pico-Green reagent and development of a fluorescence-based solution assay for double-stranded DNA quantitation. Anal. Biochem. 1997;249:228-238. DOI: 10.1006/abio.1997.2177
14. Turashvili G., Yang W., McKinney S., Kalloger S., Gale N., Ng Y., Chow K., Bell L., Lorette J., Carrier M., Luk M., Aparicio S., Huntsman D., Yip S. Nucleic acid quantity and quality from paraffin blocks: Defining optimal fixation, processing and DNA/RNA extraction techniques. Exp. Mol. Pathol. 2012;92:33-43. DOI: 10.1016/j.yexmp.2011.09.013
Выпуск
Другие статьи выпуска
В Западно-Сибирском регионе наиболее распространены грибные болезни твердой яровой пшеницы: Puccinia triticina, P. graminis, Erisiphe graminis, Tilletia caries, Ustilago tritici. Сравнительный анализ поражения проведен по сортам Алмаз, Омский рубин, Ангел, Омская янтарная. Выявлено некоторое преимущество сортов Ангел и Омская янтарная по устойчивости к бурой и стеблевой ржавчине, мучнистой росе, пыльной головне. Динамика поражения возбудителями болезней (бурой, стеблевой ржавчиной, мучнистой росой, твердой головней) представлена на примере сортов Алмаз за 1981-2022 гг. и Омский рубин за 1984-2022 гг. Динамика поражения возбудителем пыльной головни для этих же сортов представлена за 1981-2012 и1984-2012 гг. соответственно. Прослеживаются тенденции увеличения поражения бурой и стеблевой ржавчиной, мучнистой росой и снижения - твердой головней. Выявлена отрицательная связь развития возбудителя бурой ржавчины с температурой июня и суммой активных температур. С осадками и гидротермическим коэффициентом (ГТК) отмечена положительная корреляция в июне только в первой декаде, отрицательная - с температурой первой декады июля и второй декады августа. Зависимость проявления стеблевой ржавчины от метеорологических факторов наблюдалась в основном в июле: положительная корреляция - с осадками, относительной влажностью воздуха и ГТК, отрицательная - с суммой эффективных температур. В августе связь с температурой воздуха и суммой температур становится положительной, а с относительной влажностью воздуха - отрицательной со второй декады. Поражение твердой головней определяется метеорологическими условиями в мае. Обнаружена отрицательная корреляция между степенью поражения и температурой воздуха и суммой активных температур, проявляющаяся в третьей декаде мая. По пыльной головне в мае (третья декада) отмечена положительная связь с температурой воздуха и отрицательная - с относительной влажностью. В июне связь с температурой отрицательная, особенно во второй декаде, и положительная - с относительной влажностью воздуха и ГТК. В первой декаде июля (стадия колошения) связь с температурой воздуха становится положительной, а с относительной влажностью воздуха - отрицательной. Мучнистая роса в сильной степени зависит в июне от осадков и относительной влажности воздуха. В июле отрицательная связь наблюдалась с температурой воздуха и суммой эффективных температур. В августе отмечена слабая положительная связь с осадками, ГТК и отрицательная - с суммой эффективных температур. Изменения климатических условий в южной лесостепи Омской области в некоторой степени повлияли на снижение развития твердой головни пшеницы и на рост поражения мучнистой росой, бурой и стеблевой ржавчиной, пыльной головней.
Один из путей ускорения селекционного процесса основан на использовании в качестве исходных генотипов ДГ-линий (гаплоидов с удвоенным числом хромосом). В данной работе приведена характеристика по хозяйственно ценным показателям линии ДГ 48-3, которая изучалась с 2016 по 2022 г. по ускоренной селекционной схеме, начиная с селекционного питомника второго года, затем третьего (дважды) года изучения и конкурсного сортоиспытания. В результате на основе этой линии за шесть лет был создан новый сорт яровой мягкой пшеницы Сигма 5. В 2024 г. сорт включен в Государственный реестр селекционных достижений Российской Федерации по 9, 10 и 11-му регионам. Сорт Сигма 5 среднеспелый, ценный по качеству зерна, характеризуется высокой устойчивостью к листостебельным заболеваниям. Устойчивость к стеблевой ржавчине обеспечивается действием гена Sr31, к бурой ржавчине и мучнистой росе - действием генов Lr и Pm, интрогрессированных от Triticum dicoccoides. Сорт обладает высокой потенциальной продуктивностью: средняя урожайность в КСИ за 2019-2021 гг. составила 5.57 т/га. В годы массового развития ржавчинных заболеваний (2019 и 2020) его урожайность была 5.76 и 6.14 т/га соответственно, что превысило показатель неустойчивого к стеблевой ржавчине сорта-стандарта Дуэт на 3.73 и 4.05 т/га. Новый сорт превосходит сорт-стандарт и по следующим показателям качества зерна: натуре зерна, массе 1000 зерен, содержанию белка и клейковины, силе муки.
Генетические основы устойчивости мягкой пшеницы Нечерноземной зоны к возбудителю стеблевой ржавчины пшеницы, Puccinia graminis f. sp. tritici, обусловлены генами, экспрессирующими возрастной тип устойчивости, ценность которых состоит в долгосрочной защите от популяции патогена, представленной различными по вирулентности клонами гриба. В пяти сортах яровой и трех сортах озимой пшеницы, включенных в Государственный реестр селекционных достижений, допущенных к использованию, по Центральному региону РФ, с помощью метода ПЦР-анализа определены гены возрастной устойчивости к P. graminis f. sp. tritici: Sr2, Sr15, Sr22, Sr23 и Sr57. В генотипах трех сортов озимой мягкой пшеницы обнаружен ген возрастной устойчивости Sr23, сцепленный с геном устойчивости к бурой ржавчине Lr16, который встречается в селекционном материале мягкой яровой пшеницы Западной Сибири, обеспечивая эффективную защиту от ржавчинных болезней. В образцах яровой пшеницы найдены по одному-двум генам устойчивости: Sr2, Sr15, Sr22, Sr57. Фитопатологическая оценка материала в полевых условиях в сравнении со стандартами восприимчивости и устойчивости подтверждает, что сорта озимой мягкой пшеницы Московская 40, Немчиновская 24, Немчиновская 85, Сударыня, Злата, Каменка, Любава и яровой мягкой пшеницы Экада обладают качествами, способствующими получению более высокого урожая.
Козлятник широко используется в качестве лекарственного растения и на корм скоту, в биологическом земледелии и для получения биогаза. К настоящему времени в России создано 18 высокопродуктивных сортов козлятника восточного ( Galega orientalis Lam.). Активная селекционная работа продолжается, однако отсутствуют надежные методы определения сортовой и видовой принадлежности. Цель наших исследований состояла в изучении потенциала SRAP-маркеров и метода рестрикционного анализа спейсера trnH-psbA для ДНК-идентификации сортов и видов рода Galega. Исследования по оценке меж- и внутрисортового генетического полиморфизма проведены на выборке из российских сортов козлятника восточного, включенных в Госреестр селекционных достижений Российской Федерации. С использованием восьми комбинаций SRAP-праймеров получены 283 фрагмента амплифицированной ДНК, из которых 105 (37.1 %) оказались полиморфными. Эффективное число аллелей в среднем равнялось 1.37, показатель информационного содержания (PIC) - 0.787; средние значения индексов генетического разнообразия по Нею (He) и Шеннона (I) составили соответственно 0.25 и 0.41. Кластеризация образцов методом главных координат разделила их на три группы в зависимости от происхождения и хозяйственного назначения при возделывании в различных регионах. Для сортов Вест и Юбиляр, выделившихся уникальными, сортоспецифичными ампликонами, разработаны ДНК-паспорта. При амплификации с использованием практически всех комбинаций SRAP-праймеров выявлены существенные отличия в ДНК-профиле сорта Еля-Ты в сравнении с другими изучаемыми образцами. Для уточнения видовой принадлежности данного сорта был применен метод рестрикционного анализа ДНК-баркода trnH-psbA. Результаты исследования показали, что SRAP-маркеры можно успешно использовать для оценки генетического разнообразия и сортовой ДНК-идентификации козлятника восточного. Метод рестрикционного анализа спейсеров хлоропластной ДНК является эффективным подходом для различения видов в составе рода Galega.
Статистика статьи
Статистика просмотров за 2025 год.
Издательство
- Издательство
- НИИТПМ
- Регион
- Россия, Новосибирск
- Почтовый адрес
- 630089, г. Новосибирск, ул. Б. Богаткова, 175/1, Метро "Золотая нива", Автобус "Молодежная, Кошурникова"
- Юр. адрес
- 630090, г. Новосибирск, пр-т Академика Лаврентьева, 10
- ФИО
- Рагино Юлия Игоревна (Руководитель)
- Контактный телефон
- +7 (383) 3730981
- Сайт
- https://iimed.ru/